Etraviriini

| |
| |
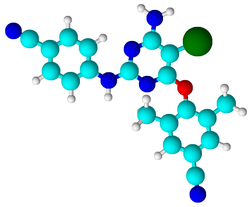
Etraviriini
| |
| Systemaattinen (IUPAC) nimi | |
| 4-[6-amino-5-bromi-2-(4-syanoanilino)pyrimidin-4-yyli]oksi-3,5-dimetyylibentsonitriili | |
| Tunnisteet | |
| CAS-numero | |
| ATC-koodi | J05 |
| PubChem CID | |
| DrugBank | |
| Kemialliset tiedot | |
| Kaava | C20H15N6BrO |
| Moolimassa | 435,28 |
| SMILES | Etsi tietokannasta: , |
| Farmakokineettiset tiedot | |
| Hyötyosuus | ? |
| Proteiinisitoutuminen | 99,9 %[1] |
| Metabolia | Hepaattinen |
| Puoliintumisaika | 41 h[1] |
| Ekskreetio | Ulosteiden mukana |
| Terapeuttiset näkökohdat | |
| Raskauskategoria |
? |
| Reseptiluokitus |
|
| Antotapa | Oraalinen |
Etraviriini (C20H15BrN6O) on bentsonitriilijohdannaisiin kuuluva orgaaninen yhdiste. Yhdiste on niin kutsuttu toisen sukupolven ei-nukleosidinen käänteiskopioijaentsyymin estäjä ja sitä käytetään lääketieteessä HIV:n hoidossa.
Vaikutusmekanismi ja käyttö
muokkaaEtraviriini sitoutuu muiden käänteiskopioijaentsyymin estäjien tavoin käänteiskopioijaentsyymiin ja estää tällöin sen DNA- ja RNA-riippuvaisen polymeraasiaktiivisuuden. Tällöin virussolut eivät pääse jakaantumaan ja kuolevat. Etraviriinia käytetään aina yhdessä muiden antiretroviraalisten lääkeaineiden kanssa. Sen on havaittu olevan tehokas myös sellaisia HIV-kantoja vastaan, jotka ovat kehittäneet resistenssin muita ei-nukleosidisia käänteiskopioijaentsyymin inhibiittoreita vastaan. Tyypillinen annostus on 200 mg/vrk ja absorptiota auttaa ruokailu lääkkeenoton jälkeen. Etraviriini tuli markkinoille vuonna 2008.[1][2][3]
Haittavaikutukset
muokkaaEtraviriinin tyypillisiä haittavaikutuksia ovat allerginen ihottuma, vatsakivut, huonovointisuus ja ripuli. Lääkeaine voi aiheuttaa myös maksan entsyymiarvojen nousua. Vuonna 2009 raportoitiin tapauksista, joissa etraviriini oli mahdollisesti aiheuttanut hengenvaarallisen Stevens–Johnson-oireyhtymän. Lääkkeellä saattaa olla myös yhteys eräisiin autoimmuunisairauksiin kuten Basedowin tautiin, polymyosiittiin ja Guillain–Barrén oireyhtymään.[1][2]
Synteesi
muokkaaEtraviriinin synteesin lähtöaineita ovat p-syanoaniliini ja syanamidi, jotka reagoivat muodostaen guanidiinijohdannaisen. Tämä reagoi dietyylimalonaatin kanssa muodostaen dihydroksisubstituoidun pyrimidiinijohdannaisen, jonka hydroksyyliryhmät korvautuvat kloorilla reaktiossa fosforyylikloridin kanssa. Näin muodostunut välituote bromataan ja yksi klooriatomeista korvautuu nukleofiilisella aromaattisella substituutiolla 2,6-dimetyyli-4-syanofenolin kanssa. Etraviriinisynteesin viimeisessä vaiheessa klooriatomi korvautuu aminoryhmällä reaktiolla ammoniakin kanssa.[4]
Lähteet
muokkaa- ↑ a b c d Paul E. Sax,Calvin J. Cohen,Daniel R. Kuritzkes: HIV Essentials, s. 163–164. Jones & Bartlett Learning, 2008. ISBN 9780763761240. Kirja Googlen teoshaussa (viitattu 10.3.2015). (englanniksi)
- ↑ a b Etravirine DrugBank. Viitattu 10.3.2015. (englanniksi)
- ↑ Raphael Dolin, Henry Masur, Michael S. Saag: AIDS Therapy, s. 484–485. Elsevier, 2007. ISBN 9781437720532. Kirja Googlen teoshaussa (viitattu 10.3.2015). (englanniksi)
- ↑ Daniel Lednicer: The Organic Chemistry of Drug Synthesis, s. 122–123. John Wiley & Sons, 2008. ISBN 978-0-470-18066-2. Kirja Googlen teoshaussa (viitattu 10.3.2015). (englanniksi)