Karbenisilliini
| |
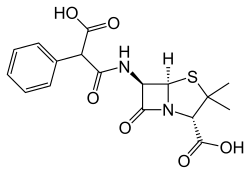
Karbenisilliini
| |
| Systemaattinen (IUPAC) nimi | |
| (2S,5R,6R)-6-[(2-karboksi-2-fenyyliasetyyli)amino]-3,3-dimetyyli-7-okso-4-tia-1-atsabisyklo[3.2.0]heptaani-2-karboksyylihappo | |
| Tunnisteet | |
| CAS-numero | |
| ATC-koodi | J01 |
| PubChem CID | |
| DrugBank | |
| Kemialliset tiedot | |
| Kaava | C17H18N2O6S |
| Moolimassa | 378,404 |
| SMILES | Etsi tietokannasta: , |
| Farmakokineettiset tiedot | |
| Hyötyosuus | 30–40 %[1] |
| Proteiinisitoutuminen | noin 50 %[2] |
| Metabolia | vähäistä |
| Puoliintumisaika | 1 tunti[2] |
| Ekskreetio | renaalinen |
| Terapeuttiset näkökohdat | |
| Raskauskategoria |
? |
| Reseptiluokitus |
|
| Antotapa | intramuskulaarinen, intravenoosi |
Karbenisilliini (C17H18SN2O6) on penisilliineihin kuuluva orgaaninen yhdiste. Sitä käytetään lääketieteessä ja eläinlääketieteessä antibioottina erityisesti Pseudomonas aeruginosa-infektioiden hoitoon, joskin nykyään sen käyttö on vähäistä.
Ominaisuudet ja käyttö
muokkaaKarbenisilliinin antibioottiset ominaisuudet perustuvat muiden penisilliinien tavoin bakteerien soluseinän synteesin estämiseen. Se on suhteellisen laajakirjoinen antibiootti. Bentsyylipenisilliiniin verrattuna se on hieman tehottomampi grampositiivisia bakteereja vastaan, mutta tehoaa penisillinaaseja tuottamattomiin kokkeihin. Karbenisilliini läpäisee paremmin gramnegatiivisten bakteerien soluseinän kuin bentsyylipenisilliini ja tehoaa erityisesti Pseudomonas aeruginosa-kantoihin. Karbenisilliini annostellaan ruiskeena ja sitä käytetään usein natriumsuolanaan. Markkinoilla on ollut myös sen aihiolääkkeitä karfenisilliiniä ja karindasiilliiniä. Lääkeainetta voidaan käyttää Pseudomonas aeruginosa-infektioiden, esimerkiksi virtsatulehdusten, hoitoon yhdessä aminoglykosidien kanssa, mutta tehokkaampi tikarsilliini on pääosin korvannut sen.[2][3][4][5][6][7]
Haittavaikutukset
muokkaaKarbenisilliini voi aiheuttaa allergiaoireita ja elektrolyyttitasapainon häiriöitä ja se on myrkyllistä maksalle.[2]
Valmistus
muokkaaKarbenisilliini on puolisynteettinen yhdiste. Sitä valmistetaan 6-aminopenisillaanihapon ja fenyylimalonihapon monobentsyyliesterikloridin välisellä reaktiolla. Bentsyyliesteriryhmä poistetaan vedyttämällä ja tuotteeksi muodostuu karbenisilliiniä.[7]
Lähteet
muokkaa- ↑ Carbenicillin DrugBank. Viitattu 20.5.2020. (englanniksi)
- ↑ a b c d M. Lindsay Grayson (päätoim.): Kucers' The Use of Antibiotics, s. 173–182. CRC Press, 2017. ISBN 9781498747967. Kirja Googlen teoshaussa (viitattu 20.5.2020). (englanniksi)
- ↑ R. J. Ponsford: Penicillins and Others, β‐Lactams, Kirk-Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, New York, 2000. (englanniksi)
- ↑ David A. Williams, William O. Foye, Thomas L. Lemke: Foye's principles of medicinal chemistry, s. 1097–1098. Lippincott Williams & Wilkins, 2012. ISBN 9781609133450. (englanniksi)
- ↑ David G. Watson: Pharmaceutical Chemistry, s. 457. Elsevier, 2011. ISBN 978-0-443-07233-8. Kirja Googlen teoshaussa (viitattu 20.5.2020). (englanniksi)
- ↑ Mark G. Papich: Saunders Handbook of Veterinary Drugs, s. 101. Elsevier, 2010. ISBN 9781437701920. Kirja Googlen teoshaussa (viitattu 20.5.2020). (englanniksi)
- ↑ a b Ṛuben Vardanyan, Victor J. Hruby: Synthesis of essential drugs, s. 440. Elsevier, 2006. ISBN 978-0-444-52166-8. Kirja Googlen teoshaussa (viitattu 20.5.2020). (englanniksi)