Riboflaviini
| |

| |
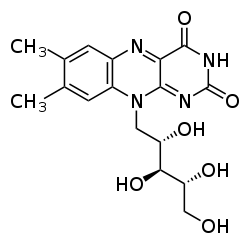
Riboflaviini
| |
| Systemaattinen (IUPAC) nimi | |
| 7,8-dimetyyli-10-[(2R,3R,4S)-2,3,4,5-tetrahydroksipentyyli]bentso[g]pteridiini-2,4-dioni | |
| Tunnisteet | |
| CAS-numero | |
| ATC-koodi | A11 |
| PubChem CID | |
| DrugBank | |
| Kemialliset tiedot | |
| Kaava | C17H20N4O6 |
| Moolimassa | 376,369 g/mol |
| Synonyymit | G vitamiini, laktoflaviini,[1] E101(i)[2] |
| Fysikaaliset tiedot | |
| Sulamispiste | 280 °C hajoaa sulamatta[3] |
| Liukoisuus veteen | liukenematon veteen (1 g/3–15 l)[1] |
| Farmakokineettiset tiedot | |
| Hyötyosuus | ~99,5 % nieltynä[4] |
| Metabolia | 60–70 % erittyy muuntumattomana, loput maksan P450:ien muuntamana[5][6] |
| Puoliintumisaika | 66–84 min nieltynä[7] |
| Ekskreetio | virtsa[6] |
| Terapeuttiset näkökohdat | |
| Raskauskategoria |
A(US); C(US) jos >1,3 mg/vrk[7] |
| Reseptiluokitus | |
| Antotapa | nieltynä, lihaspistoksena, pistoksena verenkiertoon[7] |
Riboflaviini eli B2-vitamiini on D-riboosin sitoutunut flaviini.[8] Se on yksi ihmisen tarvitsemista vitamiineista. Keho tarvitsee sitä esiasteeksi muille flaviineille: flaviinimononukleotidille (FMN) ja flaviiniadeniinidinukleotidille (FAD). FMN ja FAD sitoutuvat moniin tärkeisiin entsyymeihin näiden entsyymitoiminnan kannalta pakollisina molekyyleinä eli kofaktoreina. Näitä flaviineita sitovia entsyymeitä kutsutaan usein flavoentsyymeiksi[5] tai flavoproteiineiksi.[9]
Keho ei juuri varastoi riboflaviinia, joten sitä tulee saada usein ja kylliksi ravinnosta.[5] Riboflaviinipuutos on yleisimpiä ravintoainepuutoksia maissa, joissa syödään riisiä pääruokana ja joissa maitotuotteiden ja lihan syönti on vähäistä[10]. Myös länsimaiden vanhuksilla ja lapsilla saattaa esiintyä verrattain yleisesti lievää riboflaviinipuutosta[11].
Riboflaviinia käytetään EU:ssa elintarvikkeissa E-koodilla E101(i) väriaineena ja FMN:n natriumsuolaa koodilla E101(ii). Aineet ovat oransseja. Ruokia, joissa niitä käytetään väreinä, ovat esimerkiksi jotkin sinapit, keitot, kastikkeet, juustot ja nuudelit.[2]
Useat kasvit, bakteerit ja sienet tuottavat riboflaviinia. Se on vitamiini ihmisen lisäksi muille eläimille, sillä nekään eivät pysty valmistamaan sitä. Tosin esimerkiksi täysikasvuisilla märehtijöillä suolistobakteerit tuottavat tarpeeksi riboflaviinia, joten märehtijät eivät tarvitse sitä ravinnostaan.[12]
Suositukset ja saanti muokkaa
Riboflaviinin tarve riippuu ihmisen iästä ja sukupuolesta sekä siitä, kuinka paljon hän harrastaa fyysisiä aktiviteettejä[11].
Oheisissa taulukoissa on esitetty Suomen valtion ravitsemusneuvottelukunnan vuonna 2014 antamat ribolfaviinin saantisuositukset milligrammoina vuorokaudessa[13].
| Miehet | Naiset | ||
|---|---|---|---|
| Ikä | mg | Ikä | mg |
| 18–30 v | 1,6 | 18–30 v | 1,3 |
| 31–60 v | 1,5 | ≥ 31 v | 1,2 |
| 61–74 v | 1,4 | raskaana olevat | 1,6 |
| ≥ 75 v | 1,3 | imettävät | 1,7 |
| Pojat | Tytöt | |||||
|---|---|---|---|---|---|---|
| Ikä | mg | Ikä | mg | |||
| (Äidinmaito tai äidinmaidonkorvike tyydyttää 0-6 kk:n ikäisten ravinnetarpeet.) | ||||||
| 6–11 kk | 0,5 | 6–11 kk | 0,5 | |||
| 12–23 kk | 0,6 | 12–23 kk | 0,6 | |||
| 2–5 v | 0,7 | 2–5 v | 0,7 | |||
| 6–9 v | 1,1 | 6–9 v | 1,1 | |||
| 10–13 v | 1,3 | 10–13 v | 1,2 | |||
| 14–17 v | 1,7 | 14–17 v | 1,4 | |||
Alle 75-vuotiaat miehet saivat vuonna 2017 riboflaviinia keskimäärin 2 milligrammaa vuorokaudessa (mg/vrk) ja 0,22 mg ruuasta ravintoenergiana saatu megajoulea (mg/MJ) kohti. Alle 75-vuotiaat naiset saivat vuonna 2017 riboflaviinia keskimäärin 1,6 mg/vrk ja 0,23 mg/MJ ruuasta ravintoenergiana saatu megajoulea (mg/MJ) kohti. Miehistä 70 % sai riboflaviinia saantisuositusten mukaisesti, 18 % alle keskimääräisen tarpeen (eli alle 1,4 mg/vrk) ja 1 % alle vähimmäissaannin (eli alle 0,8 mg/vrk). Naisista 85 % sai riboflaviinia saantisuositusten mukaisesti, 9 % alle keskimääräisen tarpeen (eli alle 1,1 mg/vrk) ja 1 % alle vähimmäissaannin (eli alle 0,8 mg/vrk).[14]
Keskimääräinen tarve tyydyttää ravinnetarpeen ainoastaan puolella väestöstä, ja vähimmäissaanti viittaa tasoon, jota pienempi saanti johtaa oireilevaan puutostilaan pääosalla väestöstä.[14]
Liikasaanti muokkaa
EFSA ei ole asettanut riboflaviinin päiväsaannille ylärajaa.[15] Se on verrattain turvallinen aine, sillä keho rajoittaa sen imeytymistä tehokkaasti ja ylimäärä poistuu pääosin virtsassa.[6] Ihmisillä jopa 400 milligramman annokset nieltynä eivät ole aiheuttaneet merkittäviä haittavaikutuksia.[16]
Riboflaviini erittyy pääosin virtsassa. Syötäessä sitä suuri annos (esimerkiksi B-vitamiinitabletti) virtsa värjäytyy väliaikaisesti kellertäväksi, mutta tämä on vaaratonta. Lääketieteellinen termi tilalle on flavinuria.[17]
Riboflaviinin LD50 on rotille suun kautta tuntematon, mutta se on yli 20 grammaa per kehonpainokilogramma (g/kg).[2] LD50 pistoksena vatsaonteloon on 0,56 g/kg, jolloin rotat kuolevat riboflaviinin kiteytymiseen munuaisissa.[18]
Puutos (ariboflavinoosi) muokkaa
Riboflaviinipuutos on yleisimpiä ravintoainepuutoksia maissa, joissa syödään riisiä pääruokana ja joissa maitotuotteiden ja lihan syönti on vähäistä.[10] Puutoksen yleisin syy on ruokavalio, jossa riboflaviinia on liian vähän[10].
Riboflaviinin puutos voi aiheuttaa anemiaa, koska riboflaviini osallistuu punasolujen syntyyn, raudan imeytymiseen ja avustaa ferritiinin vapautumista kudoksista.[10] Lisäksi voi ilmetä retikulosytopeniaa (tällöin veressä on vähän epäkypsiä punasoluja), leukopeniaa (vähän valkosoluja) ja trombosytopeniaa (vähän verihiutaleita).[19]
Riboflaviinin puutosta potevilla on yleensä muitakin ravintoainepuutoksia. Ensimmäiset oireet täysin riboflaviinittomasta ruokavaliosta ilmenevät noin 3–4 kuukaudessa.[19]
Riskiryhmät muokkaa
Riboflaviininpuutosta voi esiintyä yleisesti esimerkiksi fyysisesti raskasta työtä tekevillä ja ammattiurheilijoilla maissa, joiden keskimääräinen ruokavalio sisältää vain vähän riboflaviinia.[11].
Lievä riboflaviinipuutos puutos voi olla länsimaissakin verrattain yleinen esimerkiksi vanhuksilla ja lapsilla. Kolmas riskiryhmä ovat niiden rintaruokittujen äitien vauvat, joiden riboflaviininsaanti on vähäistä. Esimerkiksi yksipuolisesti syövät kasvissyöjät ja vegaanit kuuluvat tähän ryhmään.[11] Finravinto 2017 -tutkimukseen osallistuneista miehistä 9 ja naisista 4,5 prosenttia sai liian vähän riboflaviinia[14].
Muita puutosriskiä lisääviä tekijöitä ovat maksasairaudet, eräät tartuntataudit ja alkoholismi.[10] Alkoholi estää riboflaviinin imeytymistä ja lisäksi ruokavalio on alkoholisteilla usein huono.[19] Myös jotkin hormonitoiminnan häiriöt kuten kilpirauhasen vajaatoiminta altistavat riboflaviinin puutokselle[20], koska tyroksiini lisää FAD- ja FMN-kofaktorien muodostusta. Tietyt lääkkeet kuten klooripromatsiini, imipramiini, amitriptyliini, jotkin syöpälääkkeet kuten doksorubisiini ja jotkin malarialääkkeet kuten mepakriini heikentävät kehon kykyä muuntaa riboflaviinia FAD:ksi ja FMN:ksi.[21]
Oireet muokkaa
Riboflaviinin varhaisia puutosoireita voivat olla väsymys, heikkous, suun arkuus ja kipeys, silmien kutina ja persoonallisuuden muutokset. Kaikkia varhaisia puutosoireita ei tunneta hyvin.[21]
Pidemmälle edenneessä puutoksessa oireina voivat olla väsymys; haavojen hidas parantuminen; suupielten halkeilu, punertavuus ja turvotus; sierainhaavaumat; kielen turvotus, punertavuus, halkeilu ja kipeys; ihon ja ihopoimujen paikoittainen rasvainen hilseily; silmien väsymys, punoitus, valonarkuus ja näön sumeus;[22] tuntoherkkyys ja kivut esimerkiksi käsissä ja jaloissa ääreishermoston vikatoiminnan takia.[19] Anemia ja retikulosytopenia, leukopenia ja trombosytopenia[19].
Seuraukset muokkaa
Äidin raskauden aikainen riboflaviinin puute voi aiheuttaa poikkeamia lapsen luustoon, kuten luiden lyhyyttä. Tämä voi ilmetä esimerkiksi sormien lyhyytenä.[22] Synnynnäisten sydänongelmien kehittymisen riski sikiölle voi myös kasvaa.[23]
Pitkittynyt riboflaviinin puutos lisää harmaakaihin riskiä. Tällöin mykiön proteiineja sakkautuu happiradikaalireaktioiden takia mykiöön samentaen sitä. Pelkistynyt glutationi pysäyttää radikaalireaktioita, mutta sen pelkistyminen glutationireduktaasilla vähenee FAD:n puutteen vuoksi.[10] Keho kompensoi reduktaasin vajaatoimintaa tehostamalla FAD:tä kuluttamattomalla glutationisyntetaasilla pelkistyneen glutationin tuottoa.[6]
Eläimillä muokkaa
Eläinten puutosoireet ovat osin samankaltaiset kuin ihmisillä. Rotilla ja sioilla oireita ovat mm. karvan lähtö, ihotulehdukset, hilseily ja harmaakaihi. Sioilla on myös munuaistulehduksia ja lisämunuaisten verenvuotoa. Kanoilla mm. muninta vähenee, ja kananpojille voi kehittyä koukussa olevat halvaantuneet jalat hermovaurioiden takia. Ankat kuolevat pian puutokseen. Koirilla oireita ovat mm. ihotulehdus, sydämen harvalyöntisyys, rytmihäiriöt, ataksia, harmaakaihi ja hengityksen pysähtyminen. Reesusmakakit laihtuvat, saavat iho-oireita, anemian ja kuolevat 2–6 kk kuluttua riboflaviinin saannin loppumisesta.[19]
Märehtijät, kuten naudat, eivät tarvitse yleensä riboflaviinia ravinnosta, koska niiden pötsibakteerit tuottavat riittävästi riboflaviinia. Poikkeuksena ovat mm. vastasyntyneet lampaat ja vasikat, joille ei ole vielä kehittynyt ruuansulatuselimistöön sopivaa bakteerikantaa. Nuoret yksilöt saavat tarvitsemansa riboflaviinin emän maidosta tai maitokorvikkeesta.[19]
Ruokapitoisuudet muokkaa
Eniten riboflaviinia on luontaisesti hiivauutteissa, kuten Marmitessa,[24] ja eläinten munuaisissa ja maksoissa. Sitä esiintyy erityisen runsaasti myös esimerkiksi mantelissa, kananmunassa, vehnänalkioissa, juustoissa, sian-, lampaan- ja poronlihassa, silakassa, makrillissa ja lehtikaalissa[25].
Valtaosa ruoan riboflaviinista on sen FAD:nä ja FMN:ksi kutsuttuina esiasteina, jotka ovat sitoutuneet ei-kovalenttisesti proteiineihin. Kovalenttisesti proteiineihin sitoutuneet FDA:t ja FMN:t eivät imeydy helposti, ja niitä on keskimäärin runsaammin kasveissa kuin eläimissä. Viljoissa riboflaviinista valtaosa on jyvien alkioissa ja leseissä, joten niiden poistaminen vähentää ruuan riboflaviinipitoisuutta.[5] Ruuan riboflaviinista tuhoutuu 10–20 % lihojen ja kasvisten valmistuksessa kuumentamalla ja noin 10 % leivän paistossa. Maidon pastörointi aiehuttaa noin 20 % menetyksen. Erityisen merkittävästi riboflaviinia tuhoaa maidon pitkäaikainen säilytys läpinäkyvissä astioissa valoisassa. Ruokien kuivaus ei juuri tuhoa ainetta, mutta aurinkokuivaus tuhoaa sitä runsaasti valon takia.[22]
| Lihat ja munat | Palkokasvit ja pähkinät | Viljatuotteet | |||
|---|---|---|---|---|---|
| Naudanmunuainen, pariloitu[27] | 4,58 | Soijajauho, rasvainen | 0,941 | Vehnänalkio | 0,499 |
| vasikanmaksa, paistettu[28] | 4,17 | Manteli, kuivapaahdettu | 0,599 | Vehnälese (imeytyykö?) | 0,577 |
| Kananmuna, keitetty | 0,513 | Pistaasi, kuivapaahdettu | 0,246 | Ruisjauho, täysjyvä[29] | 0,16 |
| Ankka, paahdettu | 0,47 | Cashewpähkinä, kuivapaahdettu | 0,2 | Kaurahiutale | 0,139 |
| Makrilli, savustettu | 0,35 | Pekaanipähkinä, kuivapaahdettu | 0,106 | Maissijauho, täysjyvä | 0,08 |
| Kalkkuna, nahalla, paahdettu | 0,177 | Härkäpapu, keitetty | 0,089 | Ohraryyni | 0,083 |
| Silli, säilyke | 0,139 | Kidneypapu, keitetty | 0,058 | Pasta, täysjyvä, keitetty | 0,045 |
| Kana, nahalla, paahdettu | 0,118 | Kikherne, keitetty | 0,063 | Riisi, tumma, keitetty | 0,025 |
| Kirjolohi (viljelemätön), paistettu | 0,097 | Linssi, keitetty | 0,073 | Riisi, valkoinen, keitetty | 0,013 |
| Nauta, kylki, ¼ rasvaa, pariloitu | 0,08 | Maapähkinä, kuivapaahdettu | 0,098 | Vehnäjauho, täysjyvä | 0,215 |
| Sika, jalka, vähärasvainen, paahdettu | 0,08 | Voipapu, keitetty | 0,096 | Vehnälese | 0,577 |
| Kasvikset ja ruokasienet | Hedelmät ja marjat | Lehmänmaitotuotteet | |||
| Bataatti, kuorimaton, uunipaistettu | 0,127 | Aitoviikuna | 0,05 | Briejuusto | 0,52 |
| Herne | 0,132 | Ananas | 0,036 | Camembertjuusto | 0,488 |
| Jääsalaatti | 0,03 | Appelsiini | 0,04 | Cheddarjuusto | 0,375 |
| Keltasipuli | 0,02 | Aprikoosi | 0,04 | Edamjuusto | 0,389 |
| Keräkaali, keitetty | 0,055 | Avokado | 0,122 | Maito, rasvaton | 0,14 |
| Kukkakaali, keitetty | 0,052 | Banaani | 0,1 | Raejuusto, 1 % rasvaa | 0,165 |
| Kurkku | 0,024 | Hunajameloni | 0,021 | Sinihomejuusto | 0,382 |
| Lanttu | 0,041 | Karviainen | 0,03 | Voi | 0,034 |
| Maissi, keltainen | 0,06 | Luumu | 0,096 | Kerma, 31,3 % rasvaa[27] | 0,12 |
| Parsa, keitetty | 0,126 | Mango | 0,057 | Herajauhe, makea[27] | 2,21 |
| Parsakaali, keitetty | 0,113 | Mansikka | 0,066 | Jugurtti, 3,3 % rasvaa[27] | 0,21 |
| Peruna, kuorimaton, uunipaistettu | 0,021 | Mustaherukka | 0,05 | Muut | |
| Pinaatti | 0,189 | Mustikka | 0,05 | Leivinhiiva, tuore (puristehiiva)[27] | 1,65 |
| Porkkana | 0,059 | Omena | 0,014 | Rintamaito (ihmisen) | 0,036 |
| Punajuuri, keitetty | 0,04 | Persikka | 0,041 | Olut, lager | 0,026 |
| Selleri | 0,045 | Päärynä | 0,04 | Oliiviöljy | 0 |
| Siitake, kuivattu | 1,27 | Vadelma | 0,09 | Rypsiöljy | 0 |
| Tomaatti | 0,048 | Viinirypäle | 0,02 | ||
| a: ruuat ovat raakoja eli valmistamattomia ellei toisin mainita. Pitoisuudet ovat keskimääräisiä. | |||||
Kemia muokkaa
Riboflaviini eli 7,8-dimetyyli-10-ribityyli-isoalloksatsiini on neulasmaisen kiteinen ja oranssin kellertävä aine. Sen väri alkaa tummeta noin 240 °C:n lämpötilassa. Se hajoaa sulamatta noin 280 °C:n lämpötilassa. Riboflaviini on liukenematon veteen (1 g/3–15 l vettä), dietyylieetteriin, kloroformiin, asetoniin, bentseeniin. Se on vähäliukoinen etanoliin (~45 mg/l etanolia), sykloheksaaniin, bentsyylialkoholiin ja fenoliin. NaCl:n lisäys vesiliuoksiin parantaa vesiliukoisuutta vähän. Aineen vesiliuokset ovat lievästi emäksisiä, lähes neutraaleita (pKa ~10,2). Se liukenee lievästi emäksisiin vesiliuoksiin hyvin, mutta hajoaa emäksisissä oloissa nopeasti. Valo nopeuttaa tätä hajoamista merkittävästi. Valo ei hajota riboflaviinia kuivana.[1]
Riboflaviini kestää happamissa liuoksissa hapettimia kuten vetyperoksidia, typpihappoa ja halogeenejä noin 100 °C:n lämpötilaan asti. Riboflaviini sitoo raskasmetalleja kuten Fe, Mo, Cu, Ag, Cd, Ni, Zn ja Co muodostaen voimakkaan värisiä komplekseja (metallikelaatteja). Metalli voi kiinnittyä flaviinirungon karbonyylin (=O) ja keskimmäisen renkaan vapaan typen (–N=) väliin.[8]
Riboflaviinin hajoamistuotteet ovat moninaisia ja hajoamistuoteseosten koostumus riippuu hajoamisolosuhteista. Joitakin hajoamistuotteita ovat 8-hydroksimetyyliriboflaviini (CAS-numero 52134-62-0), jota muodostuu hapettumalla; lumikromi (CAS 1086-80-2), jota muodostuu lähinnä happamassa valon vaikutuksesta; lumiflaviini (CAS 1088-56-8), jota muodostuu emäksisissä oloissa valon mahdollisesti vaikuttaessa samanaikaisesti; diasetyyli, jota muodostuu valossa hapekkaissa oloissa.[2]
| Lumikromi. | Lumiflaviini. |
Analyysi muokkaa
Useimmin käytetty riboflaviinin pitoisuuden mittausmenetelmä analysoida näyte HPLC:llä.[30]
| Vettä ja riboflaviiniliuos. | Vihreä fluoresenssi näkyy 473 nm sinisellä laserilla valaistessa. |
Riboflaviinin absorptiomaksimien aallonpituudet neutraaleissa (pH 7) vesiliuoksissa ovat 445, 372, 265 ja 220 nm. Samoissa oloissa fluoresenssimaksimit ovat 530 ja 565 nm (fluoresenssi on vihreää). Absorptiota ja emissiota voidaan käyttää hyväksi spektrofotometrisissä riboflaviinin pitoisuusmäärityksissä. Absorbanssimittaus ei ole kovin herkkä menetelmä riboflaviinin pienen absorptiokertoimen takia ja muut keltaiset aineet voivat häiritä mittausta. Herkempi menetelmä on fluoresenssimittaus. 530 nm emissio on pH 3–5:ssä lähes vakio ja ilmenee UV-valossa. Myös lumiflaviini sopii absorptio- ja emissiomittaukseen. Sen spektrofotometrinen mittaus on suoraa riboflaviinimittausta tarkempi mittaustapa. Lumiflaviinia muodostetaan säteilyttämällä näytettä fotonein. Sitten suoritetaan absorbanssimittaus 450 nm maksimin kohdalta tai fluoresenssimittaus aallonpituudella 513 nm.[30]
Pitoisuuden mittaukseen voidaan käyttää myös tiettyjen mikrobien kasvua. Ne eivät kasva, jos niiden kasvualustassa ei ole niiden tarvitsemaa riboflaviinia. Kasvunopeus ja metaboliittien määrät ovat verrannollisia riboflaviinipitoisuuteen. Esimerkiksi maitohappobakteerien kohdalla usein mitattu metaboliitti on maitohappo. Mikäli näytteessä on FAD:tä tai FMN:ää, ne voi olla välttämätöntä muuntaa riboflaviiniksi ennen mittausta. Mikrobimenetelmät ovat herkkiä ja tarkkoja.[30]
Eräs pitoisuuden mittaustapa on käyttää entsyymeitä, jotka vaativat flaviinin kofaktoriksi, ja mitata näytteestä entsyymin aktiivisuus. Tällaisesta entsyymistä on esimerkki glutationireduktaasi.[30]
Valmistus muokkaa
Teollisesti riboflaviinia tuotetaan mikrobeilla. Tietyt mikrobit tuottavat riboflaviinia aineenvaihduntatuotteena silloin, kun sitä on kasvusammiossa tarpeeksi, mikrobien kasvu pysäytetään esimerkiksi kuumentamalla. Liuos jäähdytetään. Sitten se suodatetaan ja pestään toistuvasti. Riboflaviini puhdistetaan lopuksi kiteyttämällä. Riboflaviinin tuottoon käytettyjä mikrobeja ovat muun muassa tietyt geenimuunnellut Bacillus subtilis-bakteerikannat ja Eremothecium gossypii-home.[2]
Kemiallista synteesiä ei käytetä teollisuudessa. Eräs kemiallinen synteesireitti on reagoida 3,4-ksylidiiniä ja D-riboosia metanolissa. Välituote on N-(3,4-dimetyylifenyyli)-D-1'-ribamiini. Tämä reagoi synteesin 2. vaiheessa syklokondensaatioreaktiossa barbituurihapon kanssa riboflaviiniksi. Aniliini lohkeaa reaktiossa.[2]
Toiminta eliöissä muokkaa
Tärkein riboflaviinin läpikäymä reaktio on sen kaksivaiheinen hapettuminen radikaalin kautta riboflaviinikationiksi ja päinvastainen reaktiosarja eli pelkistyminen:[5]
- riboflaviini ⇌ riboflavinyyliradikaali + H+ + e–
- riboflavinyyliradikaali ⇌ riboflaviinikationi + H+ + e–
Riboflaviinijohdannaiset FAD ja FMN toimivat eliöissä edellä kuvatulla tavalla hapetus-pelkistysreaktioissa yhden tai kahden elektronin siirtäjinä molekyyliltä toiselle. FAD:n pelkistyneiden muotojen kemialliset merkintätavat näissä siirroissa ovat FADH• ja FADH2. FMN:n muodot ovat FMNH• ja FMNH2.[31]
Eliöissä satojen eri entsyymien tiedetään sitovan flaviinin avustavana molekyylinä eli kofaktorina. Entsyymeitä voidaan kutsua flavoentsyymeiksi tai flavoproteiineiksi.[5] Näistä valtaosa sitoo FAD:n FMN:n sijaan.[21] Tietyt entsyymit sitovat molempia samanaikaisesti. Useimmat näistä entsyymeistä sitovat flaviinin väliaikaisin ei-kovalenttisidoksin, mutta jotkin myös pysyvämmin kovalenttisidosten kautta. Esimerkkejä jälkimmäisistä ovat sukkinaattidehydrogenaasi ja monoamiinioksidaasit. Kovalenttiset sidokset muodostuvat flaviinin 8-metyylin ja proteiinien histidiini- tai kysteiinitähteiden välille.[5]
Flavoentsyymit osallistuvat energiaravintoaineiden eli hiilihydraattien, aminohappojen ja lipidien aineenvaihduntaan. Joitain proteiineista tarvitaan myös pyridoksiinin ja folaattien eli B6- ja B9-vitamiinien muuntumiseen toiminnollisiksi kehossa. Riboflaviini suojaa kehoa epäsuoraan happiradikaalien reaktioilta ylläpitämällä glutationireduktaasia, joka pelkistää glutationi-antioksidanttia taas radikaalireaktioilta suojaavaan muotoon.[5]
| Flavoentsyymi | EC-numero | FAD/FMN |
|---|---|---|
| NADPH-hemoproteiinireduktaasi | 1.6.2.4 | FAD ja FMN |
| Siirtää elektroneja NADPH:lta P450:ille (EC 1.14.14.1). Pelkistää myös sytokromi c:tä ja b5:tä. | ||
| Mitokondrion elektroninsiirtoketjun kompleksi I | 7.1.1.2 (vanha: 1.6.5.3) | FMN |
| 1 elektronin siirto NADH:lta FMN:lle, jolta se siirtyy edelleen ubikinonille, joka muuntuu ubikinoliksi. | ||
| Sukkinaattidehydrogenaasi | 1.3.5.1 | FAD |
| FAD hapettaa sukkinaattia fumaraatiksi muuntuen FMNH2:ksi, joka pelkistää ubikinonia ubikinoliksi. | ||
| Glutationireduktaasi | 1.8.1.7 | FAD |
| 2 glutationia (GSH) ja NADP+ reagoivat yhdeksi glutationien disulfidiksi (GSSG) ja NADPH:ksi. | ||
| Dihydrolipoyylidehydrogenaasi | 1.8.1.4 | FAD |
| Dihydrolipoamidi ja NAD+ reagoivat disulfidisidokselliseksi lipoamidiksi ja NADH:ksi. | ||
| Monoamiinioksidaasit | 1.4.3.4 | FAD |
| Hapettaa amiineita imiineiksi siirtäen amiinien vetyjä hapelle vetyperoksidia muodostaen. | ||
| L-aminohappo-oksidaasi | 1.4.3.2 | FAD |
| Hapettaa hapen ja veden avulla (S)-aminohappoja 2-oksohapoiksi, ammoniakiksi ja vetyperoksidiksi. | ||
| Ksantiinioksidaasi | 1.17.3.2 | FAD |
| Hypoksantiinin ja ksantiinin pelkistyminen virtsahapoksi vetyperoksidia muodostaen. | ||
| Asyyli-CoA-dehydrogenaasit | 1.3.8.- (useita) | FAD |
| Hapettaa β-oksidaation 1. vaiheessa kaksoissidoksen koentsyymi A:han sitoutuneeseen rasvahappoon. | ||
Muu biokemia muokkaa
FAD:n ja FMN:n muodostus muokkaa
Riboflaviinista muodostuu FMN:ää riboflaviinikinaasilla (EC-numero 2.7.1.26). Tämä tapahtuu pääosin solulimassa. Kinaasin toimintaa kiihdyttää keskeisimmin tyroksiini. Reaktio on:[6]
FMN voi liittyä tiettyihin proteiineihin tehden niistä flavoproteiineja. Se voi myös mennä FAD-syntetaasille (EC 2.7.7.2), joka on myös tyroksiinin säätelemä. Syntetaasilla FMN:ään liittyy ATP:n adeniini, jolloin FMN:stä muodostuu FAD:[6]
- FMN + ATP ⇌ FAD + PPi
Imeytyminen muokkaa
Riboflaviini imeytyy verenkiertoon suolistosta, pääosin pohjukaissuolesta ja ohutsuolen alkupäästä. Vaikka riboflaviinin hyötyosuus suun kautta on sellaisenaan suuri (~99.5 %),[4] saattaa tiettyjen ruokien riboflaviinista imeytyä ihmisillä vain noin 60 %.[32] Ruokien proteiineihin sitoutuneet FMN:t ja FAD:t eivät nimittäin imeydy helposti. Suolistossa flavoproteiineja pilkkovat erilaiset hydrolyyttiset entsyymit, erityisesti alkaliset fosfataasit, vapauttaen siten rajatusti FAD:tä ja FMN:ää.[5] Suoliston riboflaviinin imeytymiskyky on myös rajoittunut. Suurin määrä riboflaviinia, joka sellaisenaan voi suolistosta kerta-annoksena ihmisillä imeytyä, on noin 25 mg – loput poistuvat ulosteen mukana. Etanoli estää aineen imeytymistä. Jotkin metallit ja aineet kelatoivat riboflaviinia suolistossa ja saattavat siten estää sen imeytymistä. Näitä aineita ovat esimerkiksi rauta, sinkki, kupari, nikotiinihappo, askorbiinihappo ja kofeiini.[6]
Riboflaviinin imeytyminen tapahtuu suoliston RFVT-proteiinien toimesta. Näitä on ihmisissä 3: RFVT1, RFVT2 ja RFVT3, joita koodaavat vastaavasti geenit SLC52A1, SLC52A2 ja SLC52A3. Näistä RFVT3 on ohutsuolessa yleisin.[33]
Kuljetus muokkaa
Veressä riboflaviini kulkeutuu sellaisenaan, FMN:nä ja FAD:nä.[6] Riboflaviinista noin 50 % on vetysidoksin kiinni veriplasman proteiineissa ja FMN:stä noin 80 %. Veressä nämä flaviinit sitoutuvat tiukasti fibrinogeeniin ja vasta-aineisiin, lähinnä IgA:han, IgG:hen ja IgM:ään, mutta heikosti albumiiniin. Ihmisten punasoluissa on normaalisti hyvin vähän riboflaviinia suhteessa FAD:hen ja FMN:ään, mutta syötäessä riboflaviinia yli tarpeen, sen punasolupitoisuudet kasvavat.[5]
Raskauden aikana ihmisillä ja joillain muillakin eläimillä muodostuu spesifisiä riboflaviinia sitovia proteiineja. Nämä ovat tärkeässä roolissa sikiön kehityksessä ja tiettävästi kuljettavat sikiölle riboflaviinia.[6]
Varastoituminen muokkaa
Ihmiskeho ei juurikaan varastoi riboflaviinia yli tarpeen, vaan se on kiinnittyneenä flavoproteiineihin toiminnallisen FAD:n tai FMN:n muodossa. Kehon riboflaviinista noin 60–95 % on FMN:ää ja 5–22 % on FAD:tä. Munuaisissa FAD:tä kuitenkin on noin 37 % kehon flaviineista. FAD- ja FMN-pitoisuudet ovat suurimmat maksassa, munuaisissa ja sydämessä. Riboflaviinia on sellaisenaan alle 2 % useimmissa kudoksissa paitsi verkkokalvossa. Eläinten maidossa voi tosin olla enemmän ei-toiminnallista riboflaviinia. Lehmänmaidossa löyhästi kaseiiniin sitoutuneita flaviineita on jopa 1,160–2,020 mg/l, joista valtaosa on riboflaviinia. Ihmisen maidossa taas flaviineita on 0,120–0,485 mg/l, joista valtaosa on FAD:tä ja FMN:ää. Maitopitoisuudet riippuvat riboflaviinin saannista ravinnosta. Aikuisen ihmisen keho pystyy ylläpitämään kehon toimintoja normaalisti noin 2–6 viikkoa riboflaviinin saannin loputtua kokonaan, ja sen jälkeen alkavat ensimmäiset puutosoireet.[5]
Hajotus ja erittyminen muokkaa
Riboflaviini ei tiettävästi hapetu ihmiskehossa energiaksi. Osan aineesta eliöillä käsittelee maksa. Aineen metyylit (7α- ja 8α-hiilet) hydroksyloituvat aluksi P450-entsyymeillä, jolloin ihmisellä muodostuu muun muassa 7-hydroksimetyyliriboflaviinia. Metyylit voivat hapettua edelleen ja poistua. Joidenkin eliöiden maksa myös glykosyloi riboflaviinia, jolloin muodostuu riboflaviinin α-glykosideja.[5]
Riboflaviini erittyy pääosin virtsassa. Alle 5 % poistuu ulosteessa normaaliannoksin, mutta pitoisuudet kasvavat syötäessä riboflaviinia runsaasti, ja noin 25 mg syötyä riboflaviinia on raja, jonka ylittävästä osasta kaikki loput poistuvat ulosteessa. Virtsapitoisuudet ovat ihmisillä suurimmat 2 tunnin kuluttua riboflaviinin syömisestä.[5] 60–70 % riboflaviinista erittyy virtsaan sellaisenaan. Loput erittyvät monina eri aineenvaihduntatuotteina. Näitä ovat ihmisillä muun muassa 7-hydroksimetyyliriboflaviini (10–15 % virtsan riboflaviinimetaboliiteista), 8α-sulfonyyliriboflaviini (5–10 %), 8-hydroksimetyyliriboflaviini (4–7 %) ja 10-hydroksietyyliflaviini (1–3 %).[6] Ihmisillä virtsassa ei juuri ole FMN:ää tai FAD:tä.[5]
Historia ja nimet muokkaa
Tiettävästi ensimmäisenä riboflaviinin eristi epäpuhtaana 1879 englantilainen kemisti Alexander Wynter Blyth (1844–1921). Hän eristi sen lehmänmaidon herasta ja nimesi värillisen aineen laktokromiksi (eng. lactochrome), jossa lakto viittaa maitoon ja kromi väriin. Hän ei saanut aineen rakennetta selville.[34][35][36]
Frederick Gowland Hopkins esitti vuonna 1906 julkaisemattomissa tutkimuksissaan, että maidossa on hyvin pieniä määriä tuntemattomia aineita, jotka palauttivat ruokahalun ja normalisoivat kasvun rotilla, kun niille ruokittiin puhtaista rasvoista, aminohapoista, hiilihydraateista ja suoloista koostuvaa ruokavaliota. Aineiden tiedetään olevan nykyään riboflaviinia.[37][36]
Ehkä ensimmäisenä riboflaviinipuutoksen oireita ihmisillä kuvasi lääketieteellisesti Hugh S. Stannus 1910 vangeilla Njassamaassa (nykyinen Malawi). Pellagrasta erillisiksi oireiksi hän tunnisti esimerkiksi kielen turvotuksen, suupielten haavaumat ja anemian.[38][39]
beriberiä estävää ainetta, joka nykyään tunnetaan tiamiinina (tai B1-vitamiinina), alettiin vuodesta 1916 alkaen kutsua B-vitamiiniksi. Myöhemmin sen tunnistettiin koostuvan myös pellagraa estävästä aineesta, joka tunnetaan nykyään yleisnimellä niasiini (tai B3-vitamiini). 1927 British Committee on Accessory Food Factors suositteli beriberin estäjälle nimeä B1 ja pellagran estäjälle nimeä B2.[36]
Paul György (1893–1976) osoitti vuonna 1932, että B2-vitamiinin koostuu edelleen kahdesta eri aineesta: pellagraa estävästä aineesta ja toisesta, ns. (koe-eläinten) kasvua edistävästä aineesta. Muutkin tutkijat olivat epäilleet tämän mahdollisuutta ainakin jo 1929 alkaen.[40][36] Riboflaviini tunnistettiin tästä "B2-kompleksista" ensiksi, joten sitä alettiin sittemmin kutsua B2-vitamiiniksi[36] ja niasiinille vakiintui synonyymiksi B3-vitamiini.[21]
P. György, Richard Kuhn ja Theodor Wagner-Jauregg (1857–1940) eristivät vuonna 1933 keltaisen aineen maidosta.[41][36] Pian he nimesivät sen laktoflaviiniksi (nykyään riboflaviini).[42] Pääte tulee latinan kielen sanasta keltainen, flavus.[43] Englanninkielisen sanan flavin päätteellä -in György ja kollegat halusivat kertoa, että aineessa on typpeä (vrt. amine). Pian eri lähteistä eristettiin lisää keltaisia pigmenttejä: kananmunasta eristettyä väriainetta kutsuttiin ovoflaviiniksi, maksasta eristettyä ainetta hepatoflaviiniksi jne.[42]
Kurt Günter Stern (synt. 1904) ja Ensor R. Holiday ehdottivat vuonna 1934, että flaviinit ovat isoalloksatsiineja.[44][45][36] 1933 R. Kuhn ja kollegat syntetisoivat ensimmäisinä laktoflaviinin (eli riboflaviinin).[46][47][36] Paul Karrer ja kollegat syntetisoivat saman aineen vuonna 1935 itsenäisesti.[48][36] Pian huomattiin, että vitamiineina toimiva laktoflaviini, ovoflaviini jne. ovat kemiallisesti identtisiä.[42] 1937 Yhdysvaltain lääkärijärjestön (AMA) kokouksessa nämä synonyymit hylättiin ja ainoaksi viralliseksi nimeksi valittiin riboflaviini. Etuliite ribo tulee molekyylissä olevasta D-riboosista. Nimi muutettiin, sillä esimerkiksi laktoflaviini olisi kielinyt, että aine olisi aina peräisin maidosta, mikä ei pidä paikkaansa. Myös muut vaihtoehtoiset nimet kuten G-vitamiini ja B2-vitamiini hylättiin.[49] Pian myös monet muut yhdysvaltalaisjärjestöt hyväksyivät vitamiinin ainoaksi viralliseksi nimeksi nimen riboflaviini.[42]
Lähteet muokkaa
- J. Zempleni et al.: Handbook of vitamins. 4. painos. Taylor & Francis, 2007. ISBN 9780849340222.
- G. F. Combs et al: The vitamins: fundamental aspects in nutrition and health. 3. painos. Elsevier Academic Press, 2008. ISBN 9780121834937.
- M. E. Ensminger et al.: The concise encyclopedia of foods & nutrition. CRC Press, 1995. ISBN 9780849344558.
- M. Eggersdorfer et al.: ”Vitamins”, Ullmann's Encyclopedia of Industrial Chemistry. American Cancer Society, 2000. ISBN 9783527306732. Teoksen verkkoversio.
Viitteet muokkaa
- ↑ a b c S. Budavari, M. O'Neil, A. Smith: The Merck index, s. 1304. 12. painos. Chapman & Hall Electronic Pub. Division, 2000. ISBN 9781584881292.
- ↑ a b c d e f Scientific Opinion on the re-evaluation of riboflavin (E 101(i)) and riboflavin-5′-phosphate sodium (E 101(ii)) as food additives. EFSA Journal, 2013, 11. vsk, nro 10, s. 3357. doi:10.2903/j.efsa.2013.3357. ISSN 1831-4732. Artikkelin verkkoversio. [vanhentunut linkki]
- ↑ W. M. Haynes: ”3”, CRC handbook of chemistry and physics, s. 482. 95. painos. CRC Press, 2014. ISBN 9781482208689.
- ↑ a b Dietary reference intakes for thiamin, riboflavin, niacin, vitamin B6, folate, vitamin B12, pantothenic acid, biotin and choline, s. 88, 95. National Academies Press, 2000. ISBN 9780309065542. Teoksen verkkoversio.
- ↑ a b c d e f g h i j k l m n Combs, s. 282–290
- ↑ a b c d e f g h i j Zempleni, s. 240–244
- ↑ a b c Riboflavin Drugs.com. Viitattu 7.3.2019.
- ↑ a b Eggersdorfer, s. 83–84
- ↑ Iupac: flavoproteins goldbook.iupac.org. Viitattu 19.3.2019.
- ↑ a b c d e f K. Thakur et al.: Riboflavin and health: A review of recent human research. Critical Reviews in Food Science and Nutrition, 22.11.2017, 57. vsk, nro 17, s. 3650–3660. PubMed:27029320. doi:10.1080/10408398.2016.1145104. ISSN 1549-7852. Artikkelin verkkoversio.
- ↑ a b c d H. J. Powers: Riboflavin (vitamin B-2) and health. The American Journal of Clinical Nutrition, kesäkuu 2003, 77. vsk, nro 6, s. 1352–1360. PubMed:12791609. doi:10.1093/ajcn/77.6.1352. ISSN 0002-9165. Artikkelin verkkoversio.
- ↑ A. Bacher et al.: Biosynthesis of vitamin B2 (riboflavin). Annual Review of Nutrition, 2000, 20. vsk, s. 153–167. PubMed:10940330. doi:10.1146/annurev.nutr.20.1.153. ISSN 0199-9885. Artikkelin verkkoversio. [vanhentunut linkki]
- ↑ Suomalaiset ravitsemussuositukset 2014, s. 49, 51. 5. painos. Valtion ravitsemusneuvottelukunta, 2018. ISBN 9789524538015. Teoksen verkkoversio.
- ↑ a b c L. Valsta et al.: Ravitsemus Suomessa: FinRavinto 2017 -tutkimus, s. 100. Terveyden ja hyvinvoinnin laitos, 2018. ISBN 9789523432383. Teoksen verkkoversio.
- ↑ Overview on Tolerable Upper Intake Levels as derived by the Scientific Committee on Food (SCF) and the EFSA Panel on Dietetic Products, Nutrition and Allergies (NDA) (pdf) EFSA. 2018. Viitattu 6.3.2019.
- ↑ C. Boehnke et al.: High-dose riboflavin treatment is efficacious in migraine prophylaxis: an open study in a tertiary care centre. European Journal of Neurology, heinäkuu 2004, 11. vsk, nro 7, s. 475–477. PubMed:15257686. doi:10.1111/j.1468-1331.2004.00813.x. ISSN 1351-5101. Artikkelin verkkoversio.
- ↑ Riboflavin Linus Pauling Institute. 22.4.2014. Viitattu 9.3.2019. (englanniksi)
- ↑ Opinion of the Scientific Committee on Food on the Tolerable Upper Intake Level of Vitamin B2 (pdf) 2000. Euroopan komissio. Viitattu 8.3.2019. (englanniksi)
- ↑ a b c d e f g Combs, s. 290–293
- ↑ J. A. Cimino et al.: Riboflavin metabolism in the hypothyroid human adult. Proceedings of the Society for Experimental Biology and Medicine, helmikuu 1987, 1987. vsk, nro 2, s. 151–153. PubMed:3809170. ISSN 0037-9727. Artikkelin verkkoversio.
- ↑ a b c d Zempleni, s. 234–237
- ↑ a b c Ensminger, "Chapter 18 R"
- ↑ H. P. M. Smedts et al.: Maternal intake of fat, riboflavin and nicotinamide and the risk of having offspring with congenital heart defects. European Journal of Nutrition, 1.10.2008, 47. vsk, nro 7, s. 357–365. doi:10.1007/s00394-008-0735-6. ISSN 1436-6215. Artikkelin verkkoversio.
- ↑ B. Caballero et al.: ”Volume 4”, Encyclopedia of human nutrition, s. 164. 3. painos. Elsevier, 2013. ISBN 9780123750839.
- ↑ Elintarvikkeet (haku) Fineli. Viitattu 30.10.2022.
- ↑ Combs, s. 528–560
- ↑ a b c d e Ensminger, "Chapter 6 F"
- ↑ Ensminger, "Chapter 6 F"
- ↑ Elintarvike - Fineli fineli.fi. Viitattu 30.10.2022.
- ↑ a b c d Eggersdorfer, s. 91–92
- ↑ D. L Nelson, M. M. Cox: Lehninger principles of biochemistry, s. 519. 5. painos. W. H. Freeman, 2008. ISBN 9780716771081. Teoksen verkkoversio.
- ↑ J. R. Dainty: Quantification of the bioavailability of riboflavin from foods by use of stable-isotope labels and kinetic modeling. The American Journal of Clinical Nutrition, kesäkuu 2007, 85. vsk, nro 6, s. 1557–1564. PubMed:17556693. doi:10.1093/ajcn/85.6.1557. ISSN 0002-9165. Artikkelin verkkoversio.
- ↑ V. S. Subramanian et al.: Molecular mechanisms mediating the adaptive regulation of intestinal riboflavin uptake process. PLoS ONE, 29.6.2015, 10. vsk, nro 6. PubMed:26121134. doi:10.1371/journal.pone.0131698. ISSN 1932-6203. Artikkelin verkkoversio.
- ↑ A. W. Blyth: LVI. — The composition of cows' milk in health and disease. Journal of the Chemical Society, Transactions, 1.1.1879, 35. vsk, s. 530–539. doi:10.1039/CT8793500530. ISSN 0368-1645. Artikkelin verkkoversio.
- ↑ D. T. Burns: Alexander Wynter Blyth (1844-1921). A pioneering and innovative public analyst. Journal of the Association of Public Analysts, 2007, 35. vsk, s. 17–29. Artikkelin verkkoversio. (Arkistoitu – Internet Archive)
- ↑ a b c d e f g h i C. A. Northrop-Clewes, D. I. Thurnham: The discovery and characterization of riboflavin. Annals of Nutrition & Metabolism, 2012, 61. vsk, nro 3, s. 224–230. PubMed:23183293. doi:10.1159/000343111. ISSN 1421-9697. Artikkelin verkkoversio.
- ↑ F. G. Hopkins: Feeding experiments illustrating the importance of accessory factors in normal dietaries. The Journal of Physiology, 15.7.1912, 44. vsk, nro 5–6, s. 425–460. PubMed:16993143. ISSN 0022-3751. Artikkelin verkkoversio.
- ↑ H. S. Stannus: Pellagra in Nyasaland. Transactions of The Royal Society of Tropical Medicine and Hygiene, 1.1.1912, 5. vsk, nro 3, s. 112–119. doi:10.1016/S0035-9203(12)90056-5. ISSN 0035-9203. Artikkelin verkkoversio.
- ↑ O. W. Hills et al.: Clinical aspects of dietary depletion of riboflavin. A. M. A. Archives of Internal Medicine, toukokuu 1951, 87. vsk, nro 5, s. 682–693. PubMed:14818453. ISSN 0888-2479. Artikkelin verkkoversio.
- ↑ P. György: Investigations on the vitamin B2 complex. Biochemical Journal, maaliskuu 1935, 29. vsk, nro 3, s. 741–759. PubMed:16745720. ISSN 0264-6021. Artikkelin verkkoversio.
- ↑ T. Wagner‐Jauregg, P. György, R. Kuhn: Über eine neue klasse von naturfarbstoffen (vorläufige mitteilung). Berichte der deutschen chemischen Gesellschaft, 1.2.1933, 66. vsk, nro 2, s. 317–320. doi:10.1002/cber.19330660244. ISSN 1099-0682. Artikkelin verkkoversio.
- ↑ a b c d L. E. Booher: Chemical aspects of riboflavin. Journal of the American Medical Association, 2.4.1938, 110. vsk, nro 14, s. 1105–1111. doi:10.1001/jama.1938.62790140008009. ISSN 0002-9955. Artikkelin verkkoversio.
- ↑ S. K. Schwechheimer et al: Biotechnology of riboflavin. Applied Microbiology and Biotechnology, maaliskuu 2016, 100. vsk, nro 5, s. 2107–2119. PubMed:26758294. doi:10.1007/s00253-015-7256-z. ISSN 1432-0614. Artikkelin verkkoversio.
- ↑ E. R. Holiday, K. G. Stern: Zur konstitution des photo‐flavins; versuche in der alloxazin‐reihe (vorläuf. mitteil.). Berichte der deutschen chemischen Gesellschaft, 6.6.1934, 67. vsk, nro 6, s. 1104–1106. doi:10.1002/cber.19340670637. ISSN 1099-0682. Artikkelin verkkoversio.
- ↑ K. G. Stern, E. R. Holiday: Die photo-flavine, eine gruppe von alloxazin-derivaten. Berichte der deutschen chemischen Gesellschaft, 8.8.1934, 67. vsk, nro 8, s. 1442–1452. doi:10.1002/cber.19340670832. ISSN 1099-0682. Artikkelin verkkoversio.
- ↑ P. György, R. Kuhn, T. Wagner-Jauregg: Das vitamin B2. Naturwissenschaften, 1.7.1933, 21. vsk, nro 30, s. 560–561. doi:10.1007/BF01503852. ISSN 1432-1904. Artikkelin verkkoversio.
- ↑ R. Kuhn, K. Reinemund: Über die synthese des 6.7.9-trimethyl-flavins (lumi-lactoflavins). Berichte der deutschen chemischen Gesellschaft (A and B Series), 7.11.1934, 67. vsk, nro 11, s. 1932–1936. doi:10.1002/cber.19340671132. ISSN 1099-0682. Artikkelin verkkoversio.
- ↑ P. Karrer et al.: Synthesen von flavinen III. Helvetica Chimica Acta, 1935, 18. vsk, nro 1, s. 69–79. doi:10.1002/hlca.19350180111. ISSN 1522-2675. Artikkelin verkkoversio.
- ↑ Council on pharmacy and chemistry. Journal of the American Medical Association, 17.4.1937, 108. vsk, nro 16, s. 1340–1341. doi:10.1001/jama.1937.02780160032011. ISSN 0002-9955. Artikkelin verkkoversio.
Aiheesta muualla muokkaa
- Fineli: Riboflavinin lähteet ruoka-aineissa
- Riboflaviinin kansainvälinen kemikaalikortti
- Linus Pauling Institute: Riboflavin (englanniksi)
- PubChem: Riboflavin (englanniksi)
- Human Metabolome Database: Riboflavin (englanniksi)
- DrugBank: Riboflavin (englanniksi)
- Toxin and Toxin Target Database (T3DB): Riboflavin (englanniksi)
- Kyoto Encyclopedia of Genes and Genomes (KEGG): Riboflavin (englanniksi)
- ChemBlink: Riboflavin (englanniksi)
- Food Component Database (FooDB): Riboflavine (englanniksi)
- Liber Herbarum II: Riboflaviinia sisältäviä kasveja (englanniksi)