Cahn–Ingold–Prelog-prioriteettisäännöt
Cahn–Ingold–Prelog-prioriteettisäännöt eli CIP-säännöt ovat sääntöjä, joita käytetään orgaanisessa kemiassa nimeämään eri stereoisomeereja esimerkiksi kiraalisia enantiomeereja tai kaksoissidosten E,Z-isomeriaa. Säännöt perustuvat atomien tai atomiryhmien massoihin ja ne kehittivät Robert Cahn, Christopher Kelk Ingold ja Vladimir Prelog ja he julkaisivat ne ensimmäisen kerran vuonna 1966. Prelog täydensi sääntöjä yhdessä Günter Helmchenin kanssa vuonna 1982. Cahn–Ingold–Prelog-prioriteettisääntöjen avulla orgaanisen yhdisteen stereokeskuksen stereokemia ja konfiguraatio voidaan kuvailla yksikäsitteisesti.[1][2][3][4][5][6]
Proriteettisäännöt muokkaa
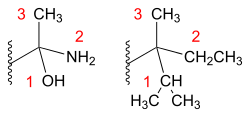
- Jokaiselle stereokeskukseen sitoutuneelle atomille tai atomiryhmälle annetaan prioriteetti ryhmän tai atomin järjestyslukujen perusteella. Mitä suurempi atomin järjestysluku, sitä korkeampi prioriteetti sillä on. Esimerkiksi hapella hiiltä raskaampana on sitä korkeampi prioriteetti.[2][3][4]
- Saman alkuaineen raskaammalla isotoopilla on suurempi prioriteetti kuin kevyemmällä isotoopilla. Esimerkiksi deuteriumin (2H) prioriteetti on suurempi kuin protiumin (1H).[3]
- Mikäli stereokeskukseen on liittynyt kaksi samaa järjestyslukua olevaa atomia, näiden keskinäisen prioriteetin määrää niihin sitoutunut prioriteetiltaan korkein atomi. Esimerkiksi -CH2CH3-ryhmä on prioriteetiltaan alhaisempi kuin -CH2CH2OH-, koska happi on prioriteetiltaan vetyä korkeampi.[2][3]
- Jokaisen atomin vetyä lukuun ottamatta valenssi on 4. Mikäli atomin valenssi on pienempi kuin 4, katsotaan sen olevan sitoutunut yhteen tai useampaan "haamuatomiin", siten että kokonaisvalenssiksi tulee 4. Näiden haamuatomien prioriteetti on 0.[3]
- Mikäli yhdisteessä on kaksois- tai kolmoissidoksia, hajotetaan ne kahdeksi tai kolmeksi yksinkertaiseksi sidokseksi.[3]
Cahn–Ingold–Prelog-prioriteettisääntöjen soveltaminen muokkaa
Cahn–Ingold–Prelog-prioriteettisääntöjä sovelletaan enantiomeerien konfiguraatioiden ja kaksoissidosten E,Z-isomeerien nimeämiseen. Enantiomeerien tapauksessa kiraalinen yhdiste piirretään siten, että prioriteetiltaan alhaisin ryhmä osoittaa katsojasta poispäin. Tämän jälkeen konfiguraatio merkitään kiertämällä korkeimmasta prioriteetista alhaisimpaan. Mikäli kiertosuunta on myötäpäivään, on kyseessä R-konfiguraatio, ja kiertosuunnan ollessa vastapäivään on kyseessä S-konfiguraatio. Kaksoissidoksellisten yhdisteiden tapauksessa prioriteetti määräytyy kaksoissidoksen atomeihin liittyneiden ryhmien prioriteettien perusteella. Mikäli kaksoissidoksen pääteatomien korkeimman prioriteetin omaavat substituentit ovat samaan suuntaan, on kyseessä Z-isomeeri, ja vastakkaisiin suuntiin on kyseessä E-isomeeri.[2][3]
Lähteet muokkaa
- ↑ CIP priority IUPAC GoldBook. IUPAC. Viitattu 17.8.2016.
- ↑ a b c d Jonathan Clayden, Nick Greeves, Stuart Warren: Organic Chemistry, s. 308–309. Oxford University Press, 2012. ISBN 978-0-19-927029-3. (englanniksi)
- ↑ a b c d e f g Michael B. Smith & Jerry March: March's Advanced Organic Chemistry, s. 138–138. John Wiley & Sons, 2013. ISBN 9780470462591. (englanniksi)
- ↑ a b Thomas Scott, Mary Eagleson: Concise encyclopedia chemistry, s. 1027. Walter de Gruyter, 1994. ISBN 978-3110114515. (englanniksi)
- ↑ R. S. Cahn, Sir Christopher Ingold & V. Prelog: Specification of Molecular Chirality. Angewandte Chemie, 1966, 5. vsk, nro 4, s. 385–415. Artikkelin verkkoversio. Viitattu 17.8.2016. (englanniksi)
- ↑ Vladimir Prelog & Günter Helmchen: Basic Principles of the CIP-System and Proposals for a Revision. Angewandte Chemie, 1982, 21. vsk, nro 8, s. 567–583. Artikkelin verkkoversio. Viitattu 17.8.2016. (englanniksi)